Añada los próximos seminarios de TIROxMDS a su calendario
En 2 rápidos pasos, puede añadir hoy mismo todo nuestro programa de próximos seminarios a su calendario. De este modo, recibirá notificaciones de las próximas conferencias, presentaciones y estudios de casos. Todos los viernes a las 8:00 AM EST, cubrimos un nuevo tema de la investigación publicada.
Añadir al calendarioPróximos seminarios web


Recomendaciones de atención
El contenido de TIRO está basado en las recomendaciones publicadas en las guías para el manejo de los nódulos tiroideos y del cáncer de tiroides . No pretenden ser "nuevas directrices". Por el contrario, la TIRO es una amalgama de recomendaciones publicadas nacidas del riguroso proceso de elaboración de directrices por parte de diversas organizaciones internacionales. Al destacar los puntos comunes y las discrepancias, pretendemos orientar al clínico sobre las normas óptimas de atención que existen actualmente.
Tablas y figuras
Haga clic en un tema para ver las tablas y figuras de esa sección.
Cáncer de tiroides diferenciado
Evaluación inicial de los nódulos tiroideos
Tablas y figuras
Tabla 4. Formas familiares y hereditarias del cáncer de tiroides
Poliposis adenomatosa familiar
| Gene | APC |
| Enfermedad tiroidea benigna | 40% |
| Cáncer | 0,4-12% |
| Tipos de cáncer | CMV-PTC: 63% FV-PTC: 25% PTC: 12% |
Tumor PTEN-Hamartoma (Cowden)
| Gene | PTEN |
| Enfermedad tiroidea benigna | 75% |
| Cáncer | 35% |
| Tipos de cáncer | PTC: 50% FV-PTC: 28% FTC: 14% |
Complejo Carney Tipo 1
| Gene | PRKARIA |
| Enfermedad tiroidea benigna | ≤ 75% |
| Cáncer | < 5% |
| Tipos de cáncer | PTC FTC |
Asociado a RET
| Gene | RET |
| Enfermedad tiroidea benigna | - |
| Cáncer | 100% |
| Tipos de cáncer | MTC |
DICER1
| Gene | DICER1 |
| Enfermedad tiroidea benigna | ≤ 30% |
| Cáncer | - |
| Tipos de cáncer | FTC FV-PTC |
CMV = Variante Morular Cribiforme; FV = Variante Folicular
Los porcentajes se refieren a la prevalencia de la enfermedad.
Sistema Bethesda
Categoría Bethesda I
| Significado | No diagnóstico |
| Riesgo estimado de malignidad | 5-10% |
Categoría Bethesda II
| Significado | Benigno |
| Riesgo estimado de malignidad | 0-3% |
Categoría Bethesda III
| Significado | Atipia de importancia indeterminada (AUS) / Lesión folicular de importancia indeterminada (FLUS) |
| Riesgo estimado de malignidad | 10-30% |
Categoría Bethesda IV
| Significado | Sospecha de neoplasia folicular (o de células de Hürthle) |
| Riesgo estimado de malignidad | 25-40% |
Categoría Bethesda V
| Significado | Sospecha de malignidad |
| Riesgo estimado de malignidad | 50-75% |
Categoría Bethesda VI
| Significado | Maligno |
| Riesgo estimado de malignidad | 97-99% |
Tal y como se recoge en The Bethesda System de Cibas y Ali (DOI 10.1007/978-3-319-60570-8).
Gestión inicial
Tablas y figuras
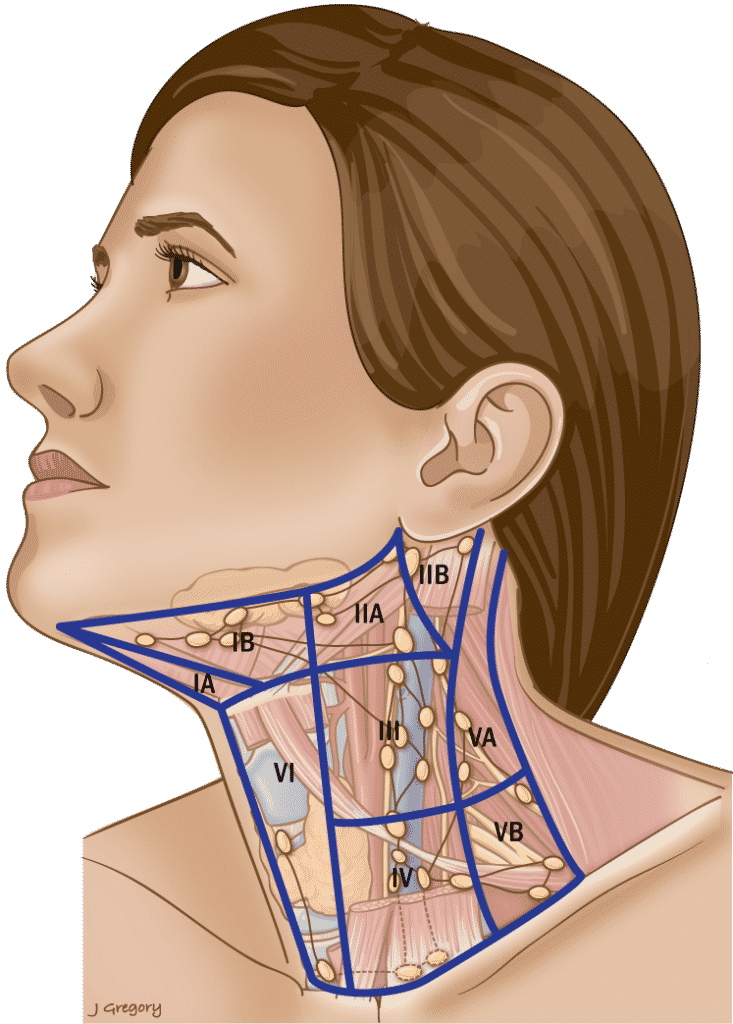
Tabla 3. Límites anatómicos de los niveles del cuello
Nivel I
| Anterior |
| Vientre anterior del músculo digástrico contralateral. |
| Posterior |
| Músculo estilohioideo |
| Superior |
| Cuerpo de la mandíbula |
| Inferior |
| Hioides |
Límites triangulares que comprenden los vientres anteriores de los músculos digástricos y los separadores del hioides IA & IB.
Nivel II
| Anterior |
| Músculo estilohioideo |
| Posterior |
| MEC posterior |
| Superior |
| Base del cráneo |
| Inferior |
| Hioides |
CN XI separa IIA & IIB. IIA Los ganglios se sitúan por delante de la VJI.
Nivel III
| Anterior |
| Músculo esternohioideo |
| Posterior |
| Músculo estilohioideo |
| Superior |
| Hioides |
| Inferior |
| Plano horizontal definido por el cartílago cricoides. |
Nivel IV
| Anterior |
| Músculo esternohioideo |
| Posterior |
| MEC posterior |
| Superior |
| Borde inferior del cartílago cricoides. |
| Inferior |
| Clavícula |
Nivel V
| Anterior |
| MEC posterior |
| Posterior |
| Borde anterior del trapecio. |
| Superior |
| Convergencia del MEC y del trapecio. |
| Inferior |
| Clavícula |
El borde inferior del cricoides se separa VA & VB.
Nivel VI
| Anterior |
| Capa anterior de la fascia cervical. |
| Posterior |
| Capa profunda de la fascia cervical. |
| Superior |
| Hioides superior |
| Inferior |
| Muesca esternal |
Nivel VII
| Anterior |
| Esternón |
| Posterior |
| Capa profunda de la fascia cervical. |
| Superior |
| Muesca esternal |
| Inferior |
| Innominado a la derecha y plano equivalente a la izquierda. |
MEC = músculo esternocleidomastoideo
Estadificación inicial y respuesta a la terapia
Etapa inicial
Tablas y figuras
Tabla 5. Estadificación AJCC del cáncer diferenciado de tiroides (mortalidad específica de la enfermedad)
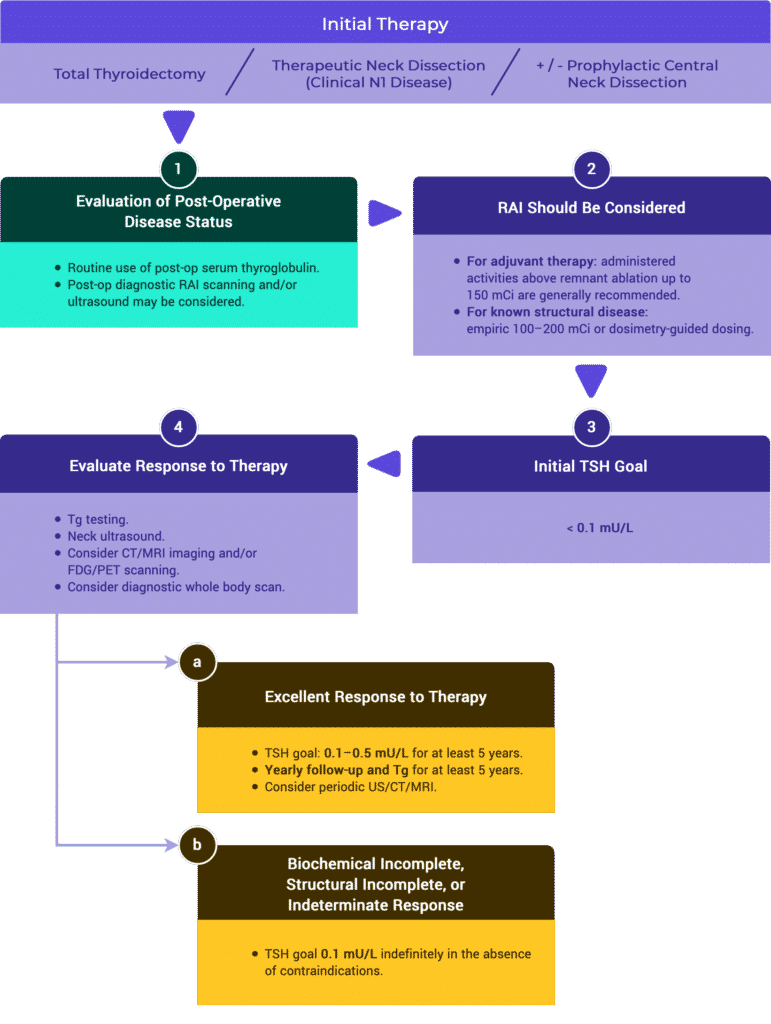
Respuesta a la terapia
Recomendaciones de gestión basadas en la estratificación del riesgo
Tablas y figuras
Tabla 11. Sistema de estratificación del riesgo con modificaciones propuestas (ATA 2009)
Nivel de riesgo
ATA Riesgo bajo
- Cáncer de tiroides papilar (con todo lo siguiente):
- No hay metástasis locales ni a distancia,
- Se ha resecado todo el tumor macroscópico,
- No hay invasión tumoral de los tejidos o estructuras loco-regionales,
- El tumor no tiene una histología agresiva (por ejemplo, célula alta, variante hobnail, carcinoma de células columnares),
- Si yo131 se da, no hay focos metastásicos ávidos de RAI fuera del lecho tiroideo en el primer escáner de RAI de cuerpo entero posterior al tratamiento,
- No hay invasión vascular,
- N0 clínico o ≤ 5 micrometástasis N1 patológicas (< 0,2 cm en su dimensión mayor).*
- Variante tiroidea folicular encapsulada e intratiroidea del cáncer papilar de tiroides.*
- Cáncer folicular de tiroides intrateracional, bien diferenciado, con invasión capsular y sin invasión vascular o con una invasión mínima (< 4 focos).*
- Microcarcinoma papilar intratiroideo, unifocal o multifocal, incluyendo BRAFV600E mutado (si se conoce).*
Riesgo intermedio ATA
- Invasión microscópica del tumor en los tejidos blandos peritiroideos.
- Focos metastásicos en el cuello con RAI en el primer escáner de cuerpo entero después del tratamiento.
- Histología agresiva (por ejemplo, célula alta, variante hobnail, carcinoma de células columnares).
- Cáncer papilar de tiroides con invasión vascular.
- N1 clínico o > 5 N1 patológico con todos los ganglios linfáticos implicados < 3 cm en su dimensión mayor.*
- Microcarcinoma papilar multifocal con ETE y BRAFV600E mutado (si se conoce).*
ATA Alto Riesgo
- Invasión macroscópica del tumor en los tejidos blandos peritiroideos (ETE bruto).
- Resección tumoral incompleta.
- Metástasis a distancia.
- Tiroglobulina sérica postoperatoria sugestiva de metástasis a distancia.
- N1 patológico con cualquier ganglio linfático metastásico ≥ 3 cm en su mayor dimensión.*
- Cáncer folicular de tiroides con invasión vascular extensa (> 4 focos de invasión vascular).*
Respuesta a la terapia basada en el manejo inicial
Tablas y figuras
Cuadro 2a. Respuesta a la terapia: Tiroidectomía total y RRA (ATA comparado con ESMO)
ATA // ESMO
Respuesta a la terapia
Excelente
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| < 0,2 ng/mL |
| TSH-Stim TG |
| < 1 ng/mL |
| TgAB |
| - No especificado (ATA) - Indetectable (ESMO) |
Bioquímica Incompleta
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| 1 ng/mL |
| TSH-Stim TG |
| 10 ng/mL |
| TgAB |
| Aumento de los niveles de TgAB |
Incompleto estructuralmente
| Imágenes |
| Evidencia de enfermedad estructural o funcional. * |
| Tg con supresión de TSH |
| * |
| TSH-Stim TG |
| * |
| TgAB |
| * |
Indeterminado
| Imágenes |
| Hallazgos inespecíficos en US/CT. - O - Débil captación en el lecho tiroideo en la exploración con RAI. |
| Tg con supresión de TSH |
| - Tg detectable, pero < 1 ng/mL (ATA) - 0,2-1 ng/mL (ESMO) |
| TSH-Stim TG |
| - Tg estimulada detectable, pero < 10 ng/mL (ATA) - 1-10 ng/mL (ESMO) |
| TgAB |
| Niveles de TgAB estables o en descenso en ausencia de enfermedad estructural o funcional. |
* Independientemente de los niveles de Tg o TgAB.
Tabla 2b. Respuesta a la terapia: Tiroidectomía total sola
ESMO
Respuesta a la terapia
Excelente
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| < 0,2 ng/mL |
| TSH-Stim TG |
| No especificado |
| TgAB |
| Indetectable |
Bioquímica Incompleta
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| Tg > 5 ng/mL - O - Valores de Tg en aumento con niveles de TSH similares. |
| TSH-Stim TG |
| - |
| TgAB |
| Aumento de los niveles de TgAB |
Incompleto estructuralmente
| Imágenes |
| Evidencia de enfermedad estructural o funcional. * |
| Tg con supresión de TSH |
| * |
| TSH-Stim TG |
| * |
| TgAB |
| * |
Indeterminado
| Imágenes |
| Hallazgos inespecíficos en US/CT. - O - Débil captación en el lecho tiroideo en la exploración con RAI. |
| Tg con supresión de TSH |
| < 0,2-5 ng/mL |
| TSH-Stim TG |
| No especificado |
| TgAB |
| Niveles de TgAB estables o en descenso en ausencia de enfermedad estructural o funcional. |
* Independientemente de los niveles de Tg o TgAB.
Cuadro 2c. Respuesta a la terapia: Lobectomía sola
ESMO
Respuesta a la terapia
Excelente
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| Estable |
| TSH-Stim TG |
| Estable |
| TgAB |
| Indetectable |
Bioquímica Incompleta
| Imágenes |
| No hay hallazgos relevantes en las imágenes. |
| Tg con supresión de TSH |
| Aumento de los valores de Tg con niveles similares de TSH |
| TSH-Stim TG |
| TgAB |
| Subiendo |
Incompleto estructuralmente
| Imágenes |
| Evidencia de enfermedad estructural o funcional. * |
| Tg con supresión de TSH |
| * |
| TSH-Stim TG |
| * |
| TgAB |
| * |
Indeterminado
| Imágenes |
| Hallazgos inespecíficos en US/CT. |
| Tg con supresión de TSH |
| * |
| TSH-Stim TG |
| * |
| TgAB |
| * |
* Independientemente de los niveles de Tg o TgAB.
Alteraciones genéticas y características histológicas
Tablas y figuras
Tabla 7. Alteraciones genéticas e histología
Fenotipo
Adenoma tóxico
Mutación genética somática conocida / Alteraciones
- TSH-R
- GNAS
Nódulos tiroideos benignos
Mutación genética somática conocida / Alteraciones
- N-, H- y K-RAS
- EIF1AX
Tumor folicular no invasivo con características similares a las del papiloma (NIFTP)
Mutación genética somática conocida / Alteraciones
- N-, H- y K-RAS
- BRAF K601E
Carcinoma papilar de tiroides infiltrativo (FVPTC)
Mutación genética somática conocida / Alteraciones
- N-, H- y K-RAS
- BRAF V600E
Carcinoma papilar de tiroides (CPT)
Mutación genética somática conocida / Alteraciones
- RET/PTC
- BRAF V600E
- N-, H-, K-RAS
- TERT
Célula columnar, célula alta, variante de PTC Hobnail
Mutación genética somática conocida / Alteraciones
- BRAF V600E
Variante de PTC difuso-escleroso
Mutación genética somática conocida / Alteraciones
- RET/PTC
Carcinoma folicular de tiroides (FTC)
Mutación genética somática conocida / Alteraciones
- N-, H- y K-RAS
- PAX8/PPAR
- PTEN
Carcinoma de células de Hürthle
Mutación genética somática conocida / Alteraciones
- NRAS
- Genes de la vía PI3K-Akt
Carcinoma de tiroides pobremente diferenciado (PDTC)
Mutación genética somática conocida / Alteraciones
- N-RAS (Insular)
- BRAF V600E
- PIK3CA
- RET/PTC
- TERT
Carcinoma anaplásico de tiroides (ATC)
Mutación genética somática conocida / Alteraciones
- N-RAS, BRAF V600E
- PIK3CA
- TP53
- β-catenina
- EIF1AX
Carcinoma medular de tiroides (CMT)
Mutación genética somática conocida / Alteraciones
- RET (Mutación de la línea germinal en el MTC heredado, mutación somática)
- N-, H- y K-RAS (mutaciones somáticas)
Adaptado con permiso de Wolters Kluwer Health, Inc.: el autor o los autores, los títulos de los artículos, el título de la revista, el número del volumen, el número del número, las páginas incluidas y la URL del sitio web de la página de la revista.
Tabla 8. Subtipos histológicos de PTC
Subtipo
Variante folicular
| ¿Presencia de las características nucleares de la PTC? |
| Sí |
| Características |
| - Mutación RAS más común. - Patrón de crecimiento folicular. |
| Pronóstico |
| 10 años DSS 93% |
Encapsulado con variante folicular, invasivo
| ¿Presencia de las características nucleares de la PTC? |
| - |
| Características |
| - La mutación RAS o el reordenamiento PPARG son más comunes. - Baja tasa de LNM. |
| Pronóstico |
| DSS de 10 años ~100% |
Variante folicular No encapsulada / Infiltrativa
| ¿Presencia de las características nucleares de la PTC? |
| - |
| Características |
| BRAF V600E más común. |
| Pronóstico |
| Equivalente a la PTC clásica/convencional |
Célula columnar
| ¿Presencia de las características nucleares de la PTC? |
| No |
| Características |
| - Papilas revestidas por células columnares con estratificación nuclear. - Los tumores grandes con invasión capsular se asocian a LNM y DM. |
| Pronóstico |
| Variable |
Morular cribiforme
| ¿Presencia de las características nucleares de la PTC? |
| Ocasionalmente |
| Características |
| - Presencia de áreas morulo-esquemáticas con inclusiones intranucleares y aclaramiento nuclear. - Asociado al síndrome de poliposis adenomatosa familiar. |
| Pronóstico |
| Equivalente a la PTC clásica/convencional |
Clásico / Convencional
| ¿Presencia de las características nucleares de la PTC? |
| Sí |
| Características |
| LNM Común |
| Pronóstico |
| - 5 años DSS 97.4% - 10 años DSS 93% |
Esclerosante difuso
| ¿Presencia de las características nucleares de la PTC? |
| Sí |
| Características |
| - Fibrosis difusa. - Infiltración linfoide densa. - Metaplasia escamosa. |
| Pronóstico |
| - 5 años DSS 96% - Equivalente al PTC de alto riesgo |
Celda alta
| ¿Presencia de las características nucleares de la PTC? |
| Sí |
| Características |
| - Posible extensión extratiroidea y LNM. - > Las células 30% son dos veces más altas que anchas y tienen un citoplasma eosinófilo. |
| Pronóstico |
| 5 años DSS 95.6% |
Hobnail
| ¿Presencia de las características nucleares de la PTC? |
| Sí |
| Características |
| - Mayor riesgo de DM. - > 30% tienen rasgos de caracol (núcleos excéntricos y citoplasma cónico). - Agrupaciones sinciciales o micropapilares con núcleos colocados apicalmente. - BRAF V600E o p53 positivo |
| Pronóstico |
| 5 años DSS 83% |
Adaptado con permiso de Wolters Kluwer Health, Inc.: el autor o los autores, los títulos de los artículos, el título de la revista, el número del volumen, el número del número, las páginas incluidas y la URL del sitio web de la página de la revista.
Uso de yodo radiactivo
Tablas y figuras
Tabla 9. Toma de decisiones sobre la ablación de remanentes
Descripción del tumor
Tumor ≤ 1 cm
| Riesgo ATA | Bajo |
| Supervivencia específica de la enfermedad mejorado por la RAI | No |
| Supervivencia sin enfermedad mejorado por la RAI | No* |
| La RAI indicó | No |
Tumor > 1-4 cm
| Riesgo ATA | Bajo |
| Supervivencia específica de la enfermedad mejorado por la RAI | No |
| Supervivencia sin enfermedad mejorado por la RAI | Datos poco claros* |
| La RAI indicó | No de forma rutinaria |
Tumor > 4 cm
| Riesgo ATA | Bajo |
| Supervivencia específica de la enfermedad mejorado por la RAI | Datos poco claros* |
| Supervivencia sin enfermedad mejorado por la RAI | Datos poco claros* |
| La RAI indicó | Considere |
Micro ETE (Cualquier tamaño de tumor)
| Riesgo ATA | Baja / Intermedia |
| Supervivencia específica de la enfermedad mejorado por la RAI | No |
| Supervivencia sin enfermedad mejorado por la RAI | Datos poco claros* |
| La RAI indicó | Considere |
Central LN Mets
| Riesgo ATA | Baja / Intermedia |
| Supervivencia específica de la enfermedad mejorado por la RAI | No |
| Supervivencia sin enfermedad mejorado por la RAI | Datos poco claros* |
| La RAI indicó | Considere |
Mets de LN laterales o mediastínicos
| Riesgo ATA | Baja / Intermedia |
| Supervivencia específica de la enfermedad mejorado por la RAI | No |
| Supervivencia sin enfermedad mejorado por la RAI | Datos poco claros* |
| La RAI indicó | Considere |
Cualquier tamaño de ETE bruto
| Riesgo ATA | Alto |
| Supervivencia específica de la enfermedad mejorado por la RAI | Sí |
| Supervivencia sin enfermedad mejorado por la RAI | Sí* |
| La RAI indicó | Sí |
Metástasis a distancia
| Riesgo ATA | Alto |
| Supervivencia específica de la enfermedad mejorado por la RAI | Sí |
| Supervivencia sin enfermedad mejorado por la RAI | Sí* |
| La RAI indicó | Sí |
* Datos observacionales contradictorios.
El editor de este material con derechos de autor es Mary Ann Liebert, Inc. publishers. Esta tabla está reimpresa y adaptada de THYROID.
Cáncer medular de tiroides
Evaluación inicial de los nódulos tiroideos sospechosos de MTC
Tablas y figuras
Tabla 12. Lo más común RET Mutaciones con riesgos asociados
RET Mutación
Nivel de riesgo más alto (HST)
M918T
| RET Exón | 16 |
| Riesgo de MTC agresivo | El más alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
Nivel de riesgo alto (H)
C634F/G/R/S/W/Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | 20-30% |
A883F
| RET Exón | 15 |
| Riesgo de MTC agresivo | Alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
Nivel de riesgo moderado (MOD)
G533C
| RET Exón | 8 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
C609F/G/R/S/Y
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C611F/G/S/Y/W
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C618F/R/S
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C620F/R/S
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C630R/Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
D631Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
K666E
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
E768D
| RET Exón | 13 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | - |
| Incidencia del hiperparatiroidismo | - |
L790F
| RET Exón | 13 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
V804L/M
| RET Exón | 14 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | 10% |
S891A
| RET Exón | 15 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | 10% |
R912P
| RET Exón | 16 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | - |
| Incidencia del hiperparatiroidismo | - |
Tabla adaptada de la Tabla 4, Wells et al, Revised ATA guidelines for the management of medullary thyroid carcinoma, Thyroid 2015. El editor de este material con derechos de autor es Mary Ann Liebert, Inc. publishers.
Gestión de los formularios heredados
Tablas y figuras
Figura 12. ATA Manejo de pacientes con RET Mutación en la línea germinal detectada en el cribado genético.
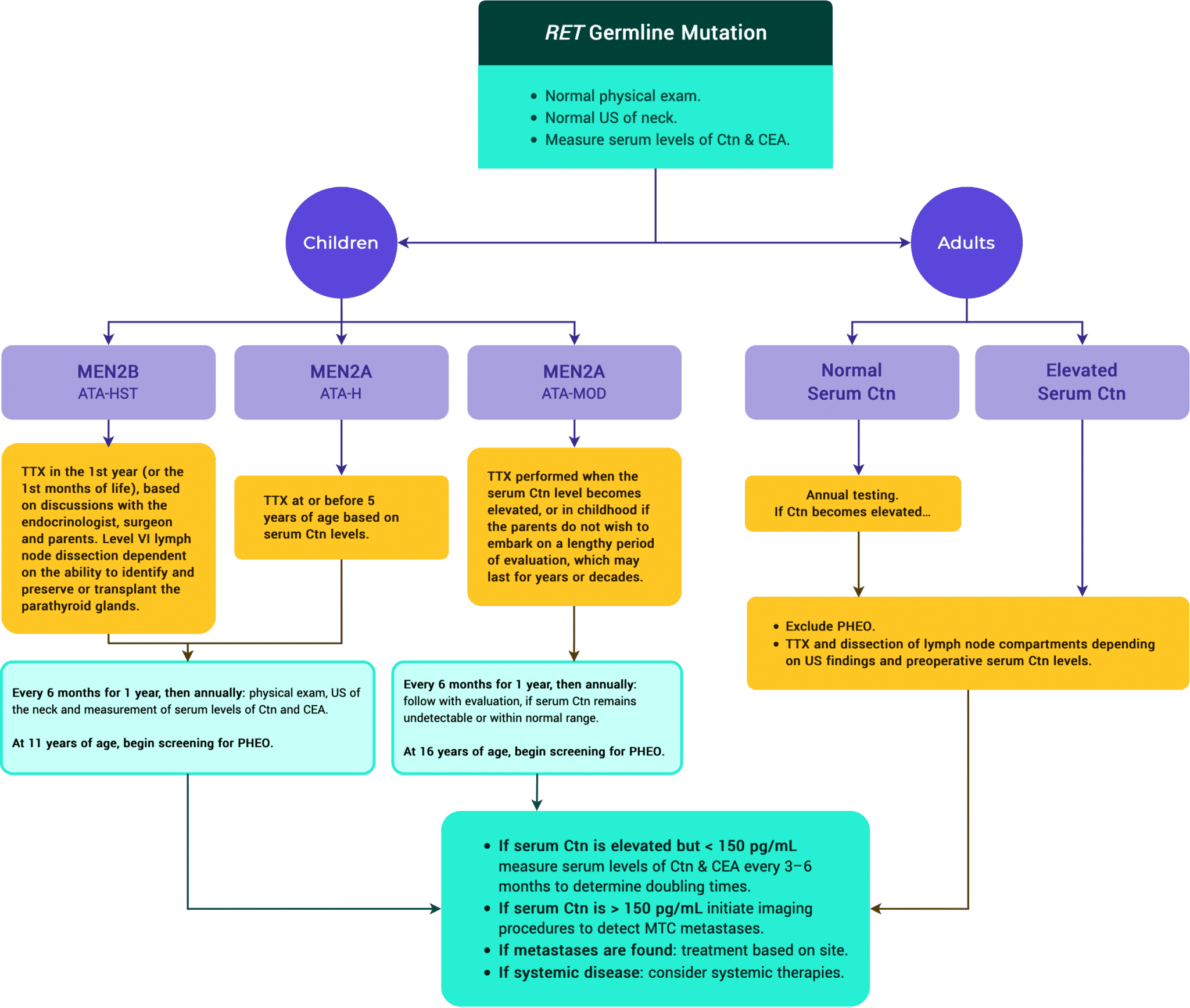
Tabla 12. Lo más común RET Mutaciones con riesgos asociados
RET Mutación
Nivel de riesgo más alto (HST)
M918T
| RET Exón | 16 |
| Riesgo de MTC agresivo | El más alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
Nivel de riesgo alto (H)
C634F/G/R/S/W/Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | 20-30% |
A883F
| RET Exón | 15 |
| Riesgo de MTC agresivo | Alto |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
Nivel de riesgo moderado (MOD)
G533C
| RET Exón | 8 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
C609F/G/R/S/Y
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C611F/G/S/Y/W
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C618F/R/S
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C620F/R/S
| RET Exón | 10 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
C630R/Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10-30% |
| Incidencia del hiperparatiroidismo | 10% |
D631Y
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 50% |
| Incidencia del hiperparatiroidismo | - |
K666E
| RET Exón | 11 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
E768D
| RET Exón | 13 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | - |
| Incidencia del hiperparatiroidismo | - |
L790F
| RET Exón | 13 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | - |
V804L/M
| RET Exón | 14 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | 10% |
S891A
| RET Exón | 15 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | 10% |
| Incidencia del hiperparatiroidismo | 10% |
R912P
| RET Exón | 16 |
| Riesgo de MTC agresivo | Moderado |
| Incidencia del feocromocitoma | - |
| Incidencia del hiperparatiroidismo | - |
Tabla adaptada de la Tabla 4, Wells et al, Revised ATA guidelines for the management of medullary thyroid carcinoma, Thyroid 2015. El editor de este material con derechos de autor es Mary Ann Liebert, Inc. publishers.
Cáncer de tiroides anaplásico
Tablas y figuras
Cuadro 16. Panel de marcadores inmunohistoquímicos de rutina
Marcador IHC
Pan-cytokeratins
| DTC | +++ |
| PDTC | +++ |
| ATC | +++/- |
| MTC | +++ |
| SCC | +++ |
| Linfoma | - |
Tiroglobulina
| DTC | +++ |
| PDTC | +/- |
| ATC | - |
| MTC | - |
| SCC | - |
| Linfoma | - |
Factor de transcripción tiroidea 1
| DTC | +++ |
| PDTC | +/- |
| ATC | -/+ |
| MTC | +/- |
| SCC | - |
| Linfoma | - |
BRAFV600E
| DTC | +/- |
| PDTC | -/+ |
| ATC | -/+ |
| MTC | - |
| SCC | - |
| Linfoma | - |
PAX8
| DTC | +++ |
| PDTC | +++ |
| ATC | +/- |
| MTC | +/- |
| SCC | - |
| Linfoma | +/-a |
Ki-67b
| DTC | < 5% |
| PDTC | 5-30% |
| ATC | > 30% |
| MTC | < 20% |
| SCC | > 30% |
| Linfoma | variable |
Cromogranina
| DTC | - |
| PDTC | - |
| ATC | - |
| MTC | +++ |
| SCC | - |
| Linfoma | - |
Calcitonina
| DTC | - |
| PDTC | - |
| ATC | - |
| MTC | +++/- |
| SCC | - |
| Linfoma | - |
Antígeno carcinembrionario
| DTC | - |
| PDTC | - |
| ATC | - |
| MTC | +++ |
| SCC | - |
| Linfoma | - |
p53
| DTC | - (raro +) |
| PDTC | -/+ |
| ATC | +/- |
| MTC | - |
| SCC | +/- |
| Linfoma | +/- |
CD45, otros marcadores linfoides
| DTC | - |
| PDTC | - |
| ATC | - |
| MTC | - |
| SCC | - |
| Linfoma | +++ |
"+" = tinción positiva relativa; "-" = tinción negativa; "+/-" = positividad variable.
a Los anticuerpos contra PAX8 pueden presentar una reacción cruzada con PAX5, que se expresa en las células linfoides.
b Porcentaje de núcleos positivos para Ki-67.
DTC = cáncer de tiroides diferenciado; IHC = inmunohistoquímica; MTC = cáncer medular de tiroides; PDTC = cáncer de tiroides poco diferenciado.
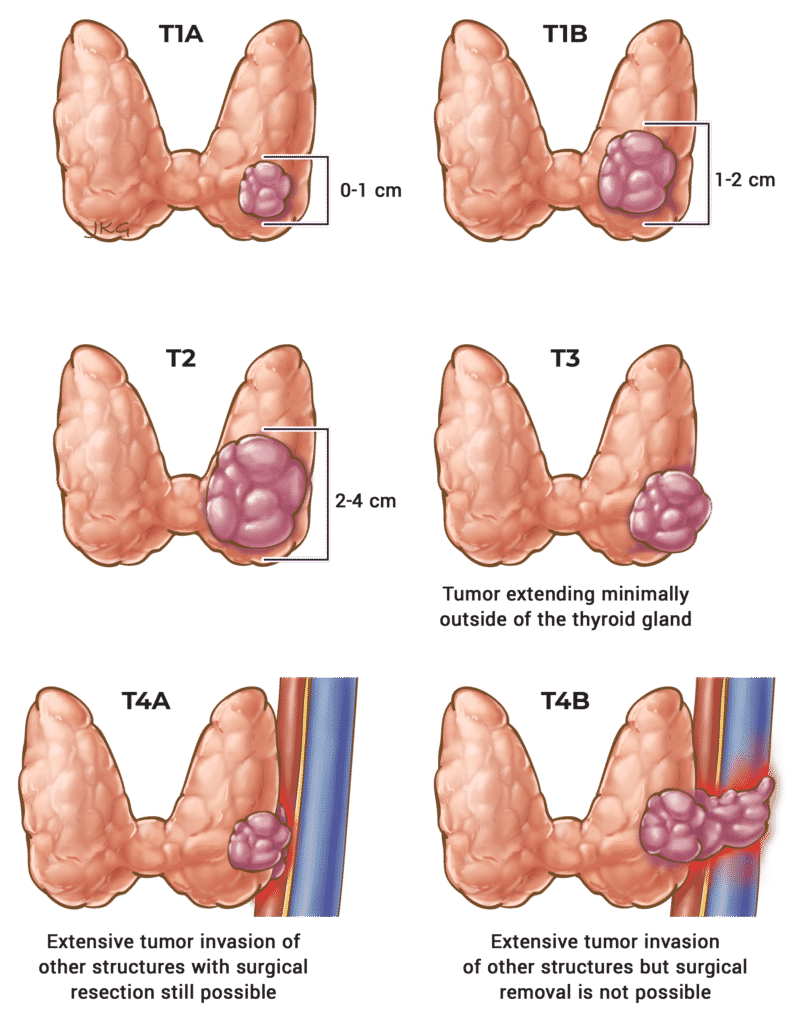
Tabla 13. T Puesta en escena para el ATC
Etapa T
T1
Descripción
< 2 cm
T2
Descripción
> 2 cm y < 4 cm
T3a
Descripción
> 4 cm
T3b
Descripción
Invasión de los músculos de la correa.
T4a
Descripción
Cáncer de cualquier tamaño con invasión de la laringe, la tráquea, el esófago o el nervio laríngeo recurrente.
T4b
Descripción
Cáncer de cualquier tamaño con extensión a las vértebras o afectación de la arteria carótida.
Adaptado de la 8ª edición del AJCC.
Tabla 14. Estadificación pronóstica del ATC
Grupo de etapas
IVA
| Etapa T | T1-T3b |
| N Etapa | N0, NX |
| Etapa M | M0 |
| Tasa de supervivencia |
IVB
| Etapa T | T1-T3a |
|---|---|
| N Etapa | N1 |
| Etapa M | M0 |
| Tasa de supervivencia |
| Etapa T | T3b |
|---|---|
| N Etapa | Cualquier N |
| Etapa M | M0 |
| Tasa de supervivencia |
| Etapa T | T4 |
|---|---|
| N Etapa | Cualquier N |
| Etapa M | M0 |
| Tasa de supervivencia |
IVC
| Etapa T | Cualquier T |
| N Etapa | Cualquier N |
| Etapa M | M1 |
| Tasa de supervivencia |
Adaptado de la 8ª edición del AJCC.
Figura 13. Algoritmo de tratamiento del ATC
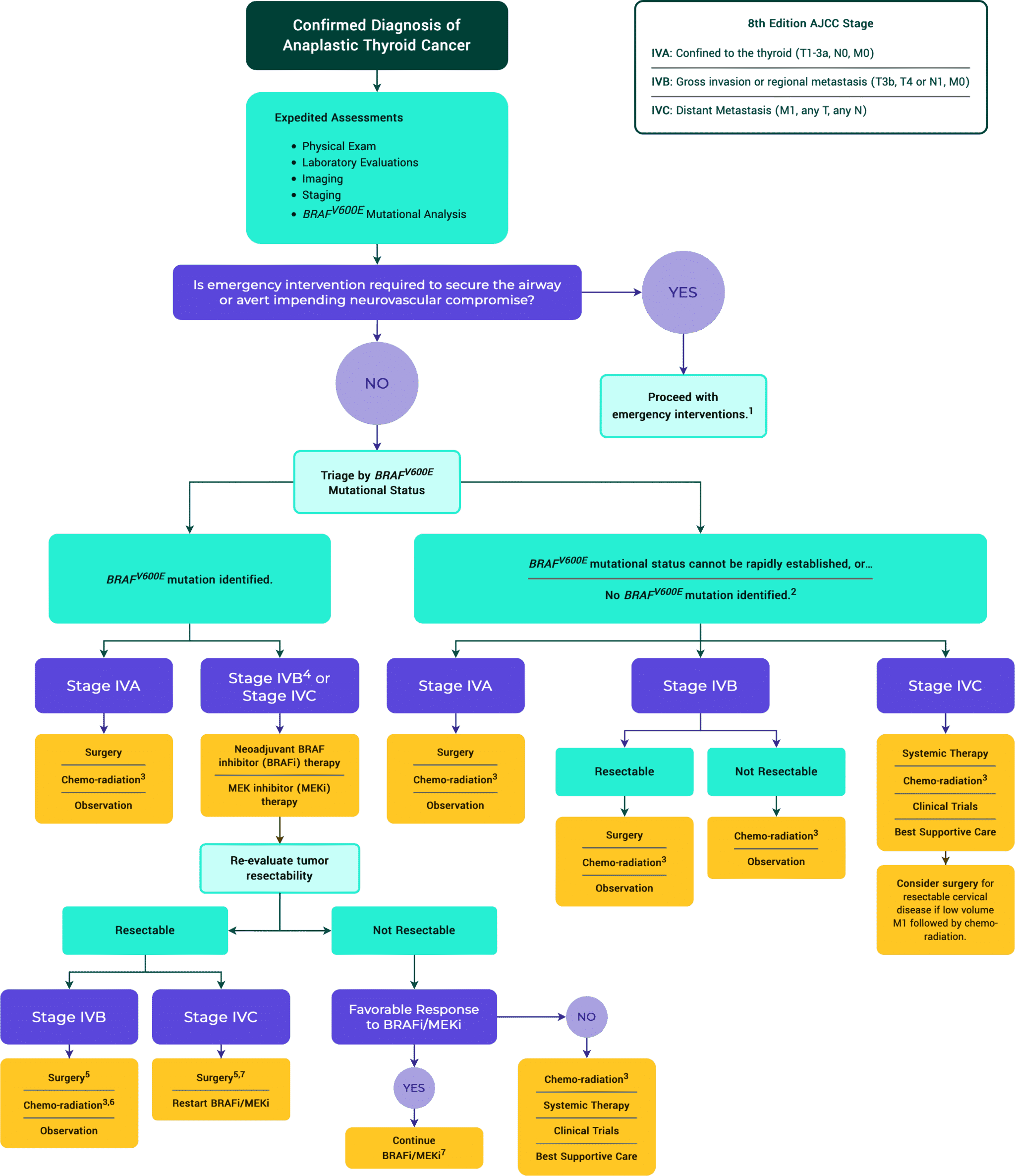
2 Se recomienda la secuenciación de próxima generación para identificar las mutaciones seleccionables. Pueden considerarse inhibidores específicos de las mutaciones de fusión oncogénicas ALK, NTRK o RET, preferiblemente en el contexto de un ensayo clínico.
3 Quimiorradiación: Normalmente, la radioterapia de intensidad modulada se administra a 70 Gy al tumor macroscópico, 60-66 Gy al lecho postoperatorio y 50-54 Gy a las posibles regiones de enfermedad residual microscópica con fraccionamiento diario estándar. La dosis de radiación puede cambiar si está clínicamente indicado. También se puede considerar un régimen de RT QUAD shot, típicamente para la enfermedad M1, (3,7Gy BID x 2 días, puede dar hasta 4-6 ciclos, permitir 1-4 semanas entre ciclos dependiendo del escenario clínico). En el MSKCC, doxorubicina 20 mg/m2 semanalmente o paclitaxel 50 mg/m2 semanal se utiliza durante todo el curso de la radiación, pero hay otros regímenes razonables descritos en la literatura.
4 Si es resecable, se puede considerar la cirugía seguida de quimiorradiación como alternativa al BRAFi/MEKi neoadyuvante.
5 Interrumpir el tratamiento con inhibidores de BRAF/Inhibidores de MEK 2 días antes de la cirugía y reanudarlo 2-3 días después de la misma.
6 Suspender el tratamiento con inhibidores de BRAF/inhibidores de MEK 2 días antes de iniciar la quimio-radiación.
7 Considerar la radioterapia si puede hacerse sin causar un retraso significativo en la terapia con inhibidores de BRAF/MEK.
Tabla 17. Mutaciones e implicaciones clínicas.
Mutaciones
BRAFV600E
Implicaciones clínicas
Comúnmente visto en DTC que puede ser precursor de ATC.
Incidencia en el ATC
40-70% de los ATC y a menudo se observa en los ATC que surgen de los PTC.
RAS
Implicaciones clínicas
Comúnmente visto en DTC que puede ser precursor de ATC.
Incidencia en el ATC
-
TP53
Implicaciones clínicas
Se considera una etapa tardía en el proceso de carcinogénesis. Se encuentra más comúnmente en el ATC.
Incidencia en el ATC
Se encuentra en el 50-70% de ATC.
TERT
Implicaciones clínicas
Se considera una etapa tardía en el proceso de carcinogénesis. Se encuentra más comúnmente en el ATC.
Incidencia en el ATC
Visto en 65-75% de ATC.
P13K/AKT
Implicaciones clínicas
Se considera una etapa tardía en el proceso de carcinogénesis.
Incidencia en el ATC
30-40% de ATC.
EIF1AX
Implicaciones clínicas
A menudo se presentan con mutaciones RAS.
Incidencia en el ATC
-
Ninguna de las mutaciones anteriores, aunque se encuentren en los ATC, es diagnóstica del ATC.
Derechos de autor y licencias
Todos los recursos creados para TIRO tienen licencia de Creative Commons Atribución-CompartirIgual 4.0 Internacional
Esta licencia exige que los reutilizadores den crédito al creador. Permite que los reutilizadores distribuyan, remezclen, adapten y construyan sobre el material en cualquier medio o formato, incluso con fines comerciales. Si otros remezclan, adaptan o construyen a partir del material, deben licenciar el material modificado bajo términos idénticos.
Esto significa que puede utilizar cualquiera de nuestras figuras o tablas en una presentación o publicación. Si lo hace, sólo tiene que dar crédito citando el siguiente texto en sus fuentes o notas a pie de página:
Ejemplo de cita
Figura 13. Algoritmo de diagnóstico del ATC. Copyright © TIRO, Fundación THANC. Todos los derechos reservados. Disponible en: https://tiro.expert

¿Qué es TIRO?
TIRO (Thyroid International Recommendations Online) es una recopilación de múltiples directrices internacionales ampliamente reconocidas sobre nódulos tiroideos y cáncer de tiroides de Estados Unidos, Europa y Japón. TIRO pone todas las directrices más actualizadas en un sitio de fácil acceso.
Además, compara y contrasta las directrices, los libros blancos y las recomendaciones internacionales sobre el cáncer de tiroides y los nódulos tiroideos de manera que se identifique dónde se alinean las directrices y dónde existen discrepancias. Actúa como un recurso dinámico para los clínicos sobre temas contemporáneos a través de clubes de revistas semanales, conferencias, juntas de tumores y mesas redondas. Este programa está dirigido por una junta multidisciplinar compuesta por los mejores especialistas en tiroides de todo el mundo.
La evidencia en el cuidado de los nódulos tiroideos y el cáncer de tiroides cambia a un ritmo rápido.
La atención basada en las directrices a menudo queda obsoleta debido a esta explosión de nuevas pruebas. TIRO (Thyroid International Recommendations Online) pone esa evidencia a disposición de los médicos en el contexto de las recomendaciones basadas en directrices.
Fácil de navegar
Comparación y contraste
Dinámico y actualizado
Acceda a las opiniones de los expertos
¿Por qué creamos TIRO?
Desarrollamos TIRO para poner las recomendaciones basadas en las directrices al alcance de los médicos que tratan a los pacientes con nódulos tiroideos y cáncer de tiroides. La directriz tiroidea de todas las directrices™.
Las actuales directrices publicadas son estáticas y de difícil acceso y navegación. TIRO se ha diseñado para resolver estos problemas y facilitar la prestación de una atención óptima al paciente en el punto de atención. Además, las directrices actuales suelen quedar obsoletas poco después de su publicación. En muchos casos, las recomendaciones publicadas se basan en pruebas menos que óptimas, así como en la opinión de expertos cuando no existen pruebas de calidad.
El objetivo de TIRO es compensar estas desventajas tradicionales. El objetivo de TIRO es proporcionar información relevante y actualizada en áreas específicas donde la evidencia es débil y donde existen discrepancias entre las guías que han sido revisadas. Este proceso se basa en la enorme cantidad de nuevos estudios que se publican en la literatura de forma regular y que se destacan en nuestras sesiones educativas virtuales semanales que se imparten y graban y luego se colocan estratégicamente en los lugares pertinentes dentro de las secciones de recomendaciones de TIRO. De este modo, pretendemos ofrecer un recurso dinámico y continuamente actualizado.
Los creadores de TIRO practican en todo el mundo
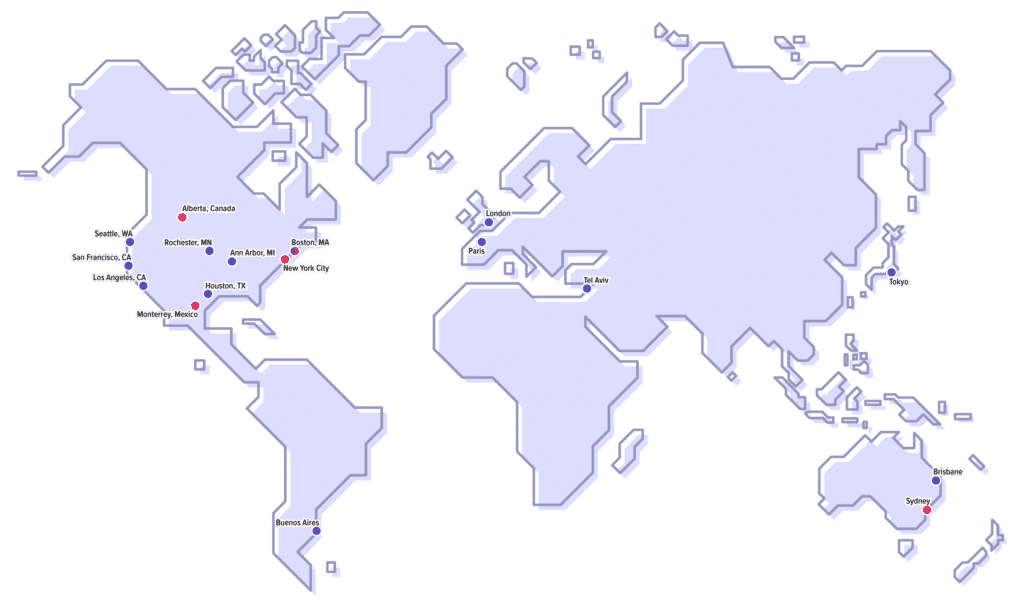
- Alberta, Canadá
- Monterrey, México
- Boston, MA
- Nueva York, NY
- Los Ángeles, CA
- San Francisco, CA
- Ann Arbor, MI
- Rochester, MN
- Filadelfia, PA
- Houston, TX
- Seattle, WA
- Buenos Aires, Argentina
- Brisbane, Australia
- Sydney, Australia
- Tokio, Japón
- París, Francia
- Tel Aviv, Israel
- Londres, Reino Unido
Cómo utilizar TIRO
El esquema clínico
Puede acceder al Esquema Clínico dentro de cualquiera de los recomendaciones de cuidado. Puede ver otras áreas de interés en la página desde el Esquema Clínico.
Para ver el esquema clínico:
- haga clic en la pestaña "i" de la parte izquierda de cualquier página de recomendación de cuidados, o
- escriba la letra "i" si está en un ordenador de sobremesa o portátil.
El esquema clínico consta de 3 partes.
Contenido de la página
Este es un índice de la sección. Aquí se muestra una estructura de alto nivel de la página, incluyendo 1st, 2nd y 3rd de nivel.
Como se ha mencionado anteriormente, puede hacer clic en cualquier parte del esquema clínico para desplazarse por la página actual.
Contenidos educativos
Esta sección muestra de un vistazo cualquier contenido nuevo y clínicamente relevante que se haya discutido o descubierto durante cualquiera de nuestros seminarios semanales. Los nuevos contenidos se añadirán de forma dinámica, en forma de videoclips. Más adelante se redactarán resúmenes en texto para facilitar los dispositivos con menor ancho de banda que puedan tener dificultades para transmitir el vídeo.
Áreas de discordia
Cuando empezamos a desarrollar TIRO, enseguida quedó claro que algunas directrices difieren sobre un tema determinado. Nos propusimos resolverlo identificando esas diferencias y contextualizándolas. Esta sección muestra, en resumen, las áreas de discordancia resumidas dentro del texto, mostradas en rojo. Además de exponer las diferencias de contenido, hemos pedido a los expertos en la materia que ofrezcan sus comentarios para aclarar las razones de las discordancias.
Tablas y figuras
Hemos creado un centro para nuestras tablas y figuras. Puede utilizarlas como referencia o en presentaciones educativas. Hemos registrado muchos de nuestros recursos en Creative Commons. Esto significa que puede utilizar ciertas figuras o tablas en una presentación o publicación. Si lo hace, simplemente cite el siguiente texto en sus fuentes o notas a pie de página.
Copyright © TIRO, Fundación THANC. Todos los derechos reservados. Disponible en: https://tiro.expert
Navegación por el sitio
Para navegar a otras páginas, puede utilizar la navegación principal -indicada por el icono de 3 líneas en la parte superior derecha- en cualquier lugar del sitio.
Para volver a la página de inicio, basta con hacer clic en el logotipo de TIRO en la parte superior de la página.